Jugendforscht Arbeit als PDF
Seminararbeit als PDF
¶ Einleitung
Wasserstoff gilt als nachhaltiger Energieträger, wenn er „sich kurzfristig von selbst erneuer[t] oder […] [seine] Nutzung nicht zur Erschöpfung der Quelle beiträgt“ (Bundesministerium für wirtschaftliche Zusammenarbeit, 2025). Dies bedeutet, dass er mittels regenerativer Ressourcen und Energien hergestellt werden muss. Hierunter können die Windkraft, die Sonnenenergie sowie die Bioenergie fallen. Diese Seminararbeit beschäftigt sich mit der Entwicklung eines Bioreaktors, der Wasserstoff mittels der Algen Chlamydomonas reinhardtii produzieren kann.
Die Algen wandeln mit Hilfe von Licht Wasser in Wasserstoff um, in beiden Fällen nicht erschöpfbare Energie- und Rohstoffquellen. „[…] Wasserstoff [kann] aus Wasser […] wiedergewonnen werden, sodaß keine Rohstoffverknappung zu befürchten ist /3/. Wasser steht praktisch in unbegrenzter Menge in den Ozeanen zur Verfügung /16/ , während die konventionellen Ressourcen von vornherein begrenzt sind.“ (Getoff, 1977). Daher handelt es sich bei diesem Verfahren um grüne Energie (vgl. Staiger & Tanţău, 2020).
Bei der Konzeption des Bioreaktors stehen drei wesentliche Faktoren im Vordergrund. Die Förderung der Nährlösung, die Lichtversorgung der Algen und die Reinhaltung des Versuchsaufbaus.
Diese Arbeit beschäftigt sich mit der Erläuterung und Diskussion der Herleitung und Herstellung sowie Programmierung des Bioreaktors, der Wasserstoff mittels der Algen Chlamydomonas reinhardtii Wasserstoff produzieren kann.
¶ Methodenteil
Im Folgenden wird das methodische Vorgehen beschrieben, wie ein Bioreaktor entwickelt wurde, der mit Hilfe der Algen Chlamydomonas reinhardtii Wasserstoff produzieren soll.
¶ Versuchsaufbau für den Algenanbau
¶ Aufbau
|
|
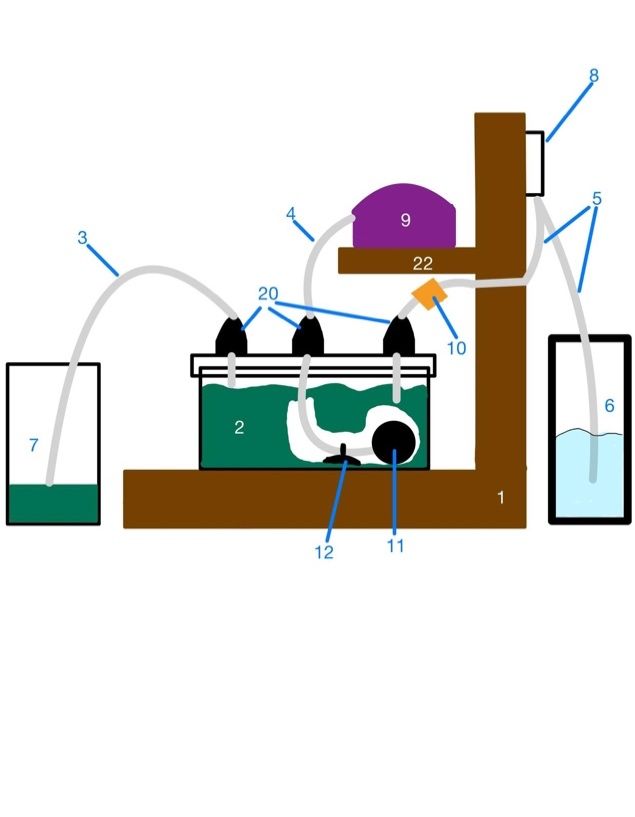
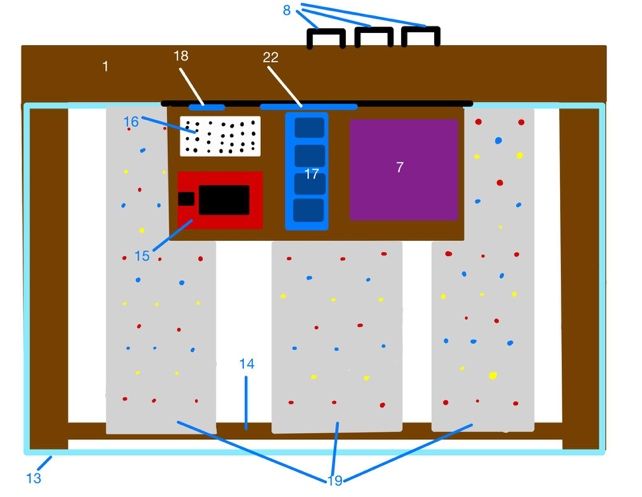
| 1: Holzgerüst | 12: Saugnapf |
| 2: Box für die Algen | 13: Glasplatte |
| 3: Schlauch für den Überfluss | 14: Holzstange |
| 4: Schlauch für die Luftzufuhr | 15: Arduino Nano mit Expansion Adapter |
| 5: Zuleitungsschläuche für die Nährlösung | 16: Breadboard |
| 6: Gefäß, das die Nährlösung enthält | 17: 5V Relais-Modul |
| 7: Überlaufs Behälter | 18: RTC Modul |
| 8: Peristaltikpumpe | 19: LED-Pflanzlampen |
| 9: Luftpumpe | 20: Kabelverschraubung |
Für den Aufbau eines Bioreaktors, der mit den Algen Chlamydomonas reinhardtii Wasserstoff produzieren soll, wurde erst ein Holzgerüst (1) gebaut. Dieses bildet die konstruktive Basis des Versuchsaufbaus. Die Algen werden in einer handelsüblichen, wasserdichten Box (2) aus Plastik gehalten. Um die Algen mit Nährstoffen versorgen zu können wurden drei Löcher mit einem Durchmesser von 13mm in den Deckel der Box gebohrt. In diese Löcher wurde anschließend jeweils eine Kabelverschraubung (20) eingelassen. Diese Verschraubungen sind mit dem Schutzfaktor IP 68 gekennzeichnet. Der Schutzfaktor bedeutet, dass die Verschraubung bei richtiger Anwendung für dauerhaftes Untertauchen in Wasser geeignet ist. Die Verschraubungen sind daher für diese Anwendung geeignet.
Jeweils eine Peristaltikpumpe (8) pro Box gewährleistet die optimale Versorgung der Algen mit Nährstoffen. Peristaltikpumpen eignen sich hierfür aufgrund ihrer Funktionsweise. Die Pumpe erzeugt einen Unterdruck am Ende des Schlauches, der sich in der jeweiligen Nährlösung befindet. Hierdurch fließt die Nährlösung, ohne dass sie mit der eigentlichen Pumpe und dadurch möglichen Schadstoffen, wie Fetten, in Berührung kommt. Auch eine Druckregulierung aufgrund unterschiedlicher Höhenniveaus ist nicht notwendig. Jede Pumpe wird in dem Holzgerüst (1) mit je zwei Schrauben befestigt. Damit die Nährlösung durch den entstehenden Druck im inneren der Box (2) nicht wieder hinaus gedrückt wird, wurde ein Rücklaufventil (10) in jedem Zuleitungsschlauch oberhalb der Box integriert.
Die Luftversorgung wird durch eine Luftpumpe (9) mit vier gleichen Ausgängen gewährleistet. Jede Box ist mit genau einem Schlauch, der mit einem Ausgang der Luftpumpe (4) verbunden ist, ausgestattet. Im Inneren der Box wird der Schlauch (4) mit Hilfe eines Saugnapfes (12) am Boden festgehalten. Am Ende des Schlauches (4) befindet sich ein Luftstein (11), der die Luft gleichmäßig in der Nährlösung verteilt und dadurch auch die Algen in Bewegung setzt. Hierdurch wird zu einem größeren Teil verhindert, dass sich die Algen zusammenschließen und somit verklumpen. Vor allem das Auszählen der Algen in einer Zählkammer wird dadurch erleichtert.
Die drei Boxen stehen auf einer Glasplatte (13), die auf den beiden Füßen des Holzgerüsts gelagert ist. In die beiden Füße ist zudem auch eine Holzstange (14) unterhalb der Glasplatten (13) eingelassen, an der die Vorderseiten den LED-Pflanzlampen (19) befestigt sind. Die Hinterseiten der Lampen werden durch den Stecker, der durch ein Loch an der Rückseite des Holzgerüsts mit den Lampen verbunden ist, gehalten. Dies ist möglich, da die Lampen ein relativ geringes Eigengewicht haben. Unter jeder Box befindet sich eine Pflanzlampe.
Der Überlaufbehälter (7) der Algen ist ein einfaches Glasgefäß. Seine einzige Aufgabe ist es, die überlaufende Nährlösung mit den Algen aufzufangen. Die Gefäße, die die Nährlösung enthalten (6), sind Schottflaschen. In diese Flaschen wird der Zuleitungsschlauch für die Nährlösung (5), der direkt zum Eingang der Peristaltikpumpe führt, in das Gefäß für die Nährlösung gefügt. Die am Flaschenhals noch existierende Lücke wird anschließend mit Parafilm abgedichtet, sodass die Nährlösung möglichst ohne Kontamination während des Versuches verbleibt.
Die Steuerung der drei Peristaltikpumpen (8) erfolgt durch einen Arduino Nano mit Expansion Adapter (15), einem Breadboard (16), einem RTC-Modul (18), einem 2x16 LCD-Display mit I2C-Modul (21) und dem 5V-Relais-Modul (17). Die genannten Bauteile werden mit Hilfe von Schrauben mit einem Durchmesser von 3mm und dazu passenden Unterlegscheiben an dem Zwischenboden (22) und der Wand des Holzgerüsts befestigt. Zudem wird in das RTC-Modul eine 3 V-Knopfzelle eingelegt. Die für den Aufbau verwendeten Komponenten sind im Anhang 1 aufgeführt.
¶ Schaltung
Für die Verbindung der einzelnen Bauteile mit dem Mikrocontroller wurden Steckbrückenverbindungen verwendet. Der Arduino Nano wurde auf den Expansion Adapter aufgesetzt. Für das Verbinden der Peristaltikpumpen mit dem 5V Relais-Modul und den Lüsterklemmen auf den DC-Buchse Adapter wurde rotes Litzenkabel für die positiven Polungen und schwarzes Litzenkabel für die negativen Polungen verwendet.
Der SDA-Pin des LCD-Displays und des RTC-Moduls wurden über das Breadboard mit dem A4 Pin des Expansion Adapters verbunden. Der SCL-Pin des LCD-Displays und des RTC-Moduls wurden auch über das Breadboard mit dem A5 Pin des Expansion Adapters verbunden. Der VCC-Pin beider Anbauteile wurde direkt mit einem 5 V Pin des Expansion Adapters verbunden. Genauso wurde auch der GND-Pin beider Bauteile mit einem beliebigen GND-Pin des Expansion Adapters verbunden. Die Relais wurden auf einem 5V-Relais-Modul befestigt. Dieses Modul steuert das gewünschte Relais an. Der VCC- und der GND-Pin des Moduls wurden mit den entsprechenden Pins auf dem Expansion Adapter verbunden. Jedes Relais verfügt über einen eigenen Input Pin. Die Input Pins 1-3 wurden hier verwendet. Dabei ist der Input Pin 1 mit dem D2 Pin des Expansion Adapters, der Input Pin 2 mit dem D3 Pin des Expansion Adapters und der Input Pin 3 mit dem D4 Pin des Expansion Adapters verbunden.
Die Minuspole der drei Peristaltikpumpen wurden direkt mit dem „Lüsterklemme auf DC-Buchse“-Adapter verbunden. Der Adapter wiederum ist an ein 12 V-Netzteil angeschlossen. Die Pluspole der Peristaltikpumpen sind durch schraubbare Anschlussklemmen mit dem Verbraucherausgang NO (Normally Open) verbunden. Um den Stromkreis zu schließen wurde der COM Ausgang mit dem Pluspol der Lüsterklemmen des DC-Buchse Adapters verbunden. Die Verbindung mit dem Verbraucherausgang NO hat den Vorteil, dass die Pumpen durch Abschalten des Mikrocontrollers den Pumpvorgang beginnen, da die Relais ohne den nötigen Impuls des Microkontrollers den Stromkreis der Pumpen automatisch schließen. Dadurch ist ein Test sowie eine Reinigung der Zuleitungsschläuche für die Nährlösung möglich.
¶ Programmierung
Das Programm wurde in der Programmierumgebung „Arduino-IDE“ geschrieben.
Das Programm steuert über die drei Pins D2, D3, D4 die Relais der drei Peristaltikpumpen. Die zeitliche Steuerung der Relais erfolgt über das RTC-Modul. Das RTC-Modul stellt dem Mikrocontroller die aktuelle Uhrzeit zur Verfügung, selbst wenn dieser vom Strom getrennt wird. Hierfür wird das LCD-Display mit I2C-Modul für die sekundengenaue Ausgabe der Uhrzeit sowie dem Schriftzug „Es wird gepumpt!“, der beim Pumpen erscheint, genutzt. Der Schriftzug dient der Kontrolle und dem Nachvollziehen des Prozesses, den der Microkontroller ausführt.
Beim Hochfahren des Systems initialisiert das Programm das LCD-Display und das RTC-Modul. Hierfür wurden die Pins D2, D3 und D4 als Ausgänge gesetzt. Falls das RTC-Modul vorher keinen Strom hatte, wird es auf eine vordefinierte Uhrzeit gesetzt. Die Batterie eines solchen RTC-Moduls versorgt dieses bis zu fünf Jahre mit Strom, was für die Versuchsdurchführung ausreichend ist.
Nach dem Initialisieren aller Variablen wir eine Schleife gestartet. Diese überprüft sekündlich die aktuelle Systemuhrzeit und gibt diese auch am LCD-Display aus. Wenn die Schleife den Beginn einer vollen Stunde erkennt, werden die Pumpen für einen definierten Zeitraum aktiviert und es erscheint auf dem LCD-Display der Schriftzug „Es wird gepumpt!“. Beim Erkennen einer vollen Stunde wird sowohl die Sekunde und die Minute des RTC-Moduls abgefragt. Wenn beide Parameter gleich Null sind, beginnt eine neue volle Stunde und jedes einzelne Relais wird für seinen zuvor definierten Zeitraum aktiviert. Hierdurch fördern die Peristaltikpumpen genau 5 mL.
Um den Entwicklungsprozess effizienter zu gestalten wird außerdem auf dem seriellen Monitor die aktuelle Uhrzeit und der Pumpenstatus wiedergegeben. Hierdurch kann man die Aktionen des Mikrocontrollers direkt nachvollziehen und Fehler sowie Probleme in der Hard- und Software erkenne sowie gegebenenfalls lösen. Der genaue Programmcode ist im Anhang 3 wiedergegeben.
¶ Kalibrierung
Damit der Bioreaktor genau arbeitet, müssen die Pumpen kalibriert werden, sodass sie exakt 5mL pro Stunde pumpen.
Dafür wurden die Pumpen zuerst auf Schwachstellen getestet. Die benutzten Pumpen wurden bereits nach wenigen Minuten im Betrieb warm, wodurch die Pumpleistung abfällt. Somit konnten sie nicht in einer einfachen Testreihe kalibriert werden.
Stattdessen wurde das Programm so geschrieben, dass die Pumpen jede Stunde eine Minute lang pumpen. Im Anschluss wurde die geförderte Wassermenge gemessen.
Bei einer Belastung von einer Minute wiesen die Pumpen keinen Leistungsabfall auf. Durch zehnmalige Wiederholung konnte ein möglichst genauer Durchschnittswert berechnet werden. Die Zeit, die die Pumpen laufen, wird im Programm in Millisekunden angegeben. Dadurch mussten die errechneten Werte teilweise auf Millisekunden aufgerundet werden, da der Arduino keine Nachkommastellen im Millisekundenbereich unterstützt.
Um 5 mL pro Stunde zu fördern, laufen die Pumpen ca. 2 Sekunden pro Stunde. Dadurch entsteht kaum Hitze, die somit kein Problem darstellt.
Um wirklich zu testen, ob die Pumpen korrekt arbeiten, wurde der Bioreaktor ohne Boxen für die Algen in Betrieb genommen. Die Messung lief über drei Tage und es wurde die Wassermenge immer erst nach einigen Stunden mit Hilfe einer Küchenwage gemessen, da herkömmliche Messbecher für die Wassermengen zu ungenau wären.
¶ Absorption des Lichtes als Fehlerquelle
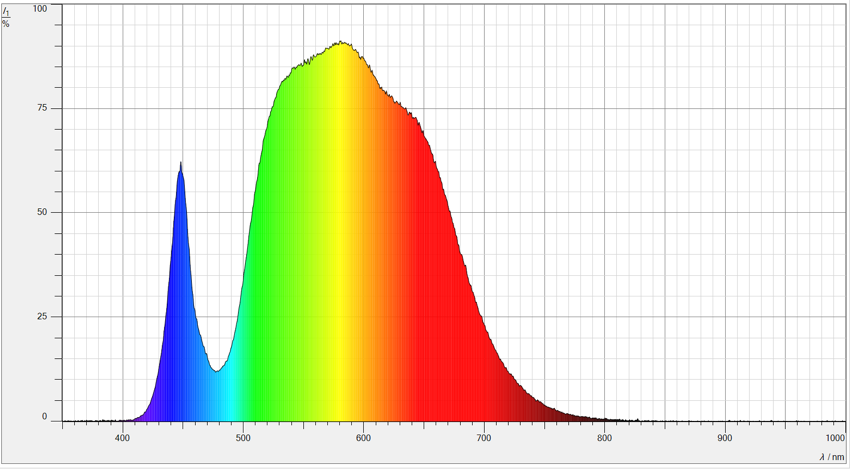
Eine Fehlerquelle des Versuchaufbaus kann die Beleuchtung der Algen durch die LED-Pflanzlampen darstellen, da das Licht sowohl durch die Glasplatte als auch durch die Box gelangen muss. Dabei können Spektren, die für die Algen wichtig sind, absorbiert werden. Um dies zu untersuchen, wurde mit einem Photospektrometer im gleichbleibenden Abstand von 10 cm zur LED-Pflanzlampe hin zuerst ausschließlich das Spektrum der LED-Pflanzlampe gemessen. Anschließend wurde der Versuch mit der LED-Pflanzlampe und der Glasplatte wiederholt sowie mit der LED-Pflanzlampe, der Glasplatte und der Plastikbox. Der Messpunkt des Spektrometers lag bei der letzten Messung mit der Box innerhalb der Box, da dort auch die Algen angezüchtet werden. Die LED-Pflanzlampen wurden auf die sechste von neun Helligkeitsstufen eingestellt. Die neunte Stufe ist die höchste Helligkeitsstufe, allerdings liegt die Intensität aller Stufen über der sechsten außerhalb des Messbereichs des Spektrometers. Die Spektren wurden anschließend in dem dafür vorgesehen Programm ausgegeben. Das verwendete Spektrometer sowie Programm sind im Anhang 4 zu finden.
¶ Versuchsaufbau der Abfüllautomation
|
 |
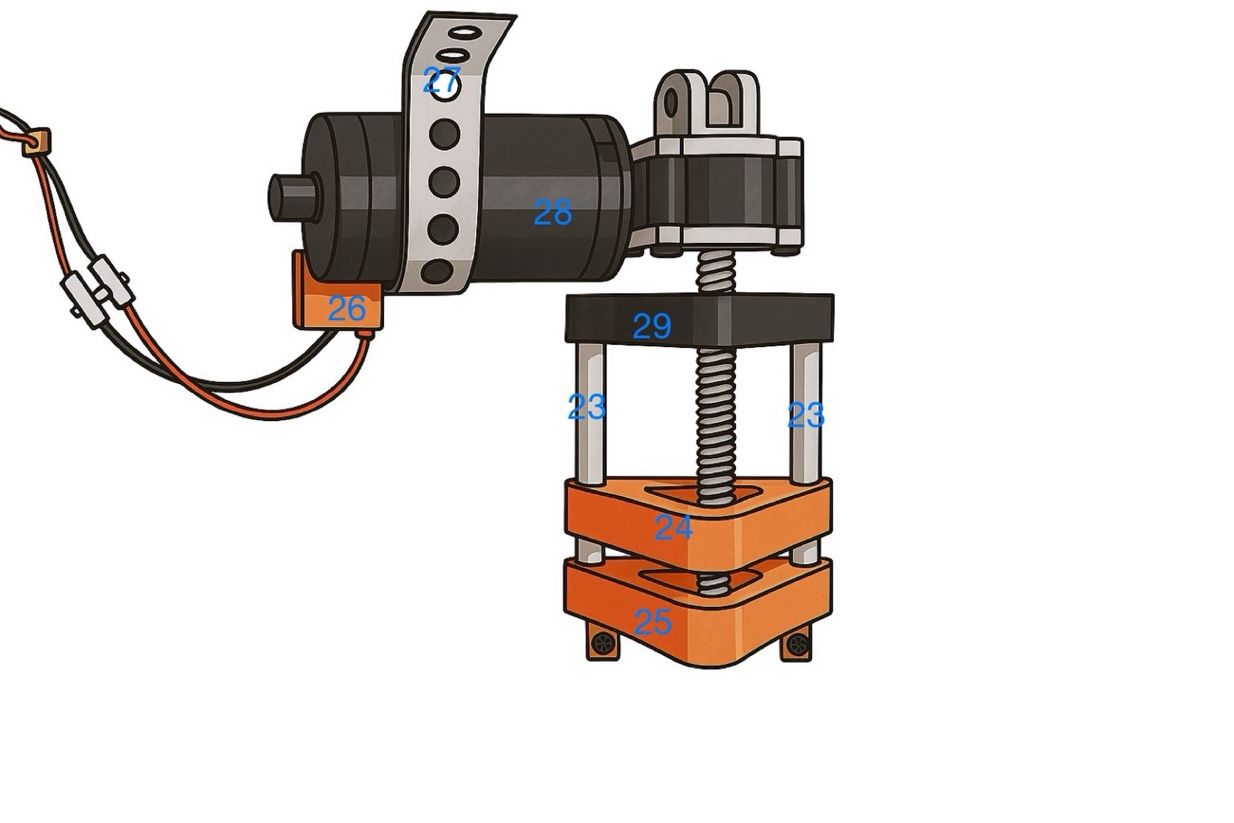
| 23: Edelstahlstäbe (Ø10mm) | 27: Montageband (20mm breit) |
| 24: bewegliche Plattform | 28: 12 V Getriebemotor mit Spindel |
| 25: Unterer Boden/Deckel für Flasche | 29: Oberer Boden |
| 26: Clip zum befestigen der Kontakte | 30: Deckel mit Gewinde |
| 31: 100 mL Headspaceflasche mit Bördelrand |
Damit die Algen luftdicht verschlossen sind und kein Wasserstoff bei der Entschwefelung entweichen kann, müssen sie in eine Headspaceflasche mit Bördelrand (31) abgefüllt werden. Die Headspaceflasche hat ein Volumen von 100mL. Um dies zu erreichen, muss der Gummistopfen der verschlossenen Flaschen mit einer Nadel durchstochen werden. Die entwickelte Abfüllautomation kann dies umsetzen. Dafür wird ein 12 V Getriebemotor mit Spindel (28) verwendet, der mit dem Ende der Spindel in einer dafür vorgesehen Einkerbung in dem unteren Boden (25) gelagert ist und durch ein 12 mm breites Loch im oberen Boden (29) durchgeführt wird. Durch Aktivieren des Motors dreht sich die Spindel in die entsprechende Richtung, sodass sich die bewegliche Plattform (24) durch ein Gewinde, das in ihr eingelassen ist, hoch und runter fahren lässt. Zudem kommen zwei 9cm lange Edelstahlstäbe (23) als Führungsschiene zum Einsatz. Die Edelstahlstäbe wurden im unteren und oberen Boden in 10 mm tiefen Löchern mit einem Radius von 11 mm mit Sekundenkleber verklebt. Die Toleranz von 1mm ist für die Fertigung der Böden im 3D-Drucker von Relevanz.
Auf die Kontakte des Getriebemotors wurde jeweils eine Flachsteckhülse gesteckt, damit möglichst einfach ein Kabel angelötet werden und der Motor jederzeit abgesteckt werden kann. Um zu verhindern, dass die Flachsteckhülsen von den Kontakten des Getriebemotors abfallen, wurde ein Clip (26) entworfen, der die Hülsen auf den Kontakten fixiert. Dieser wurde ebenfalls in 3D-gedruckt.
Der untere Boden (25) wird durch zwei Schrauben an der Wand des Holzgerüsts (1) fixiert und der Getriebemotor (28) mit dem Montageband (27) an dem Zwischenboden (22) verschraubt.
Um nun Algen abfüllen zu können wird eine Nadel, an der ein Schlauch befestigt ist, mit einer Verschraubung mittig in die bewegliche Plattform (24) eingespannt. Der Schlauch der Nadel wird durch ein Loch in der Mitte des oberen Bodens (29) durchgeführt. So kann auf Knopfdruck problemlos durch das Gummi gestochen werden.
Der Deckel der Headspaceflasche wird mit einem Gewinde, das ebenfalls in 3D-gedruckt ist, in den unteren Boden (25) hineingeschraubt. Das Gewinde wird in zwei Teilen gedruckt, die anschließend mit Sekundenkleber an dem Verschluss der Flasche geklebt werden. Durch das Hineinschrauben der Flasche in den unteren Boden sitzt die Flasche stabil und kann weder verrutschen noch hinausfallen.
Um die Algen in die Flasche hineinzupumpen werden drei weitere Peristaltikpumpen verwendet. Diese werden ebenfalls in dem Holzgerüst verschraubt. Um diese drei Peristaltikpumpen anzusteuern wird je Pumpe ein Schalter verwendet. Das Anbringen eines Messstrichs an der Headspaceflasche stellt sicher, dass eine bestimmte Menge von Algen abgefüllt werden kann. Es wird bis zum Messstrich abgefüllt und durch die Pumpe entstehende Hitzeprobleme mit entsprechendem Leistungsabfall sind nicht relevant.
Alle selbsterstellten 3D-Dateien sind auf dem beigelegten USB-Stick zu finden.
¶ Konstruieren des Gewindes für die bewegliche Plattform
Damit die bewegliche Plattform hoch und runter gefahren werden kann benötigt sie ein passendes Gewinde, für die Spindel des 12 V Getriebemotor. Da die Spindel kein genormtes Gewinde hat musste ein passendes konstruiert werden. Hierfür wurde in dem Programm „Autodesk Fusion 360“ die „Spirale“ Funktion ausgewählt, um das Gewinde in die bewegliche Plattform einzulassen. Da aber das Gewinde nicht bekannt war, musste es experimentell über mehrere Versuche bestimmt werden. Als Basiseinstellung wurde hierbei die Einstellung „Dreieckig (extern)“ gewählt, die einem Gewinde ähnelt. Zudem wurde der Ort des Gewindes auf der beweglichen Plattform an die Lagerung sowie der Öffnung für die Spindel und den beiden Edelstahlstäben angepasst.
Um das passende Gewinde zu ermitteln, wurden insgesamt neun Testdrucke angefertigt. Zu Beginn der Versuchsreihe wurden zwei komplette Gewinde gedruckt, die sich ausschließlich durch einen unterschiedlichen Innendurchmesser unterschieden. Da sich diese Methode als ineffizient erwies wurden die nächsten vier Gewinde in Querschnitten angefertigt und mit jedem 3D-Druck wurde das Gewinde abgeändert. Dabei wurden zu Beginn größere Schritte verwendet, die anschließend immer kleiner und präziser wurden. Für die beiden finalen Anpassungen wurde das Gewinde im Ganzen aber ohne die gesamte bewegliche Plattform abgeändert.
¶ Ergebnisse
¶ Kalibrierung der Peristaltikpumpen
Die Peristaltikpumpen wurden in einer Testreihe mit zehnmaliger Wiederholung getestet. Hierbei weist die erste Peristaltikpumpe eine Standardabweichung von 1,0%, die zweite Peristaltikpumpe eine Standardabweichung von 1,3% und die dritte Peristaltikpumpe eine Standardabweichung von 2,1% auf. Die erhobenen Messungen und Rechnungen sind in der Tabelle im Anhang 2 aufgelistet.
Der anschließende Testdurchlauf des Bioreaktors (siehe Abbildung 4) wies eine Abweichung von ca. 0,1 mL pro Stunde der errechneten Fördermenge von 5mL auf. Auch fielen im weiteren Forschungsbetrieb keine Ausfälle der Pumpen auf.

¶ Auswertung der Absorption des Lichtes
|
|
|
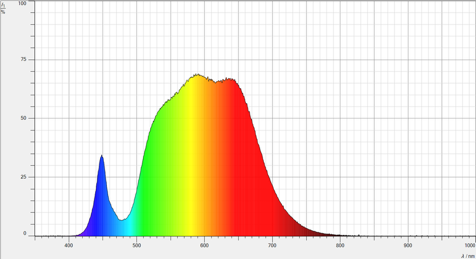
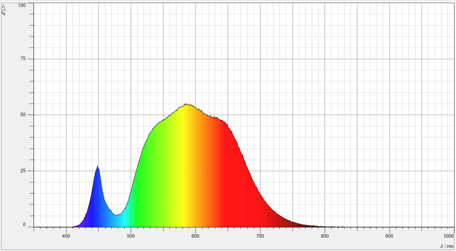
Hier sind die drei gemessenen Spektren zu sehen. Zuerst wurde das reine Spektrum der LED-Pflanzlampen ermittelt. Danach erfolgte die Aufnahme des Spektrums durch die Glasplatte und danach das Spektrum durch die Glasplatte und Box zusammen. Es fällt auf, dass die einzelnen Komponenten keinen bestimmten Bereich des Spektrums absorbieren, sondern viel mehr die gesamte Intensität der LED-Pflanzlampe hemmen.
¶
Ermittlung des Gewindes für die bewegliche Plattform
Für die Abfüllautomation ist es besonders wichtig, dass die bewegliche Plattform gleichmäßig auf und ab fährt. Dafür ist das passende Gewinde von höchster Relevanz. Das wurde in neun Durchgängen ermittelt. Dabei wuchs die Steigung von 2 mm auf 3,2 mm an. Der innere Durchmesser wurde auf 9 mm angepasst und der äußere auf 14,5 mm. Auch änderte sich die Schnittgröße der Spirale von 3 mm auf 4 mm im Laufe der Versuche. Die Größe des Gewindes musste aufgrund des Programmes „Autodesk Fusion 360“ auf 20 mm festgelegt werden, da ansonsten nicht durch die gesamte Dicke der Plattform, die 17 mm beträgt, das Gewinde geschnitten und sich die Spindel ansonsten festsetzen würde.
¶ Diskussion
¶ Kalibrierung der Peristaltikpumpen
Die Peristaltikpumpen erwiesen sich im Betrieb als sehr zuverlässig. Durch die kurze Beanspruchung der Pumpen von ca. zwei Sekunden pro Stunde entsteht kaum bis keine Wärme, die die Pumpen verlangsamen könnte. Durch das stündliche Fördern der Nährlösung sind die Standartabweichungen zu vernachlässigen, da sie zum einen relativ gering ausfallen und ein Versuchsdurchgang zwei Wochen dauert wodurch sich die leichten Abweichungen in der Fördermenge ausgleichen und die Ergebnisse nicht beeinflusst werden.
Der dreitägige Test des Bioreaktors mit Wasser verfälscht den Bioreaktor ebenfalls nicht, da die später verwendete Nährlösung zu 99% aus Wasser besteht und die darin enthaltenen Salze vollständig gelöst sind. Der Flüssigkeitsverlust der Pumpen in der dreitägigen Testreihe sowohl durch Verdunstung und durch die Messungenauigkeit der Waage erklären. Der errechnete Verlust von 0,1 mL pro Pumpvorgang würde dies auch bestätigen, da es nur Verluste an Wasser gab und nie einen Überschuss. Zudem ist der Flüssigkeitsverlust so gering, dass er im regulären Betrieb des Bioreaktors nicht von bedeutender Relevanz ist und somit das Ergebnis der Forschung an den Algen nicht nachweisbar verfälscht.
¶ Absorption des Lichtes und Tauglichkeit der LED-Pflanzlampen

Bei der Auswertung der drei Spektren konnte trotz Hinzufügen der Glasplatte und der Box keine Absorption bestimmter Spektren des Lichtes festgestellt werden. Lediglich die gesamte Intensität des Lichtes nahm beim Hinzufügen der einzelnen Komponenten ab, wie in den Abbildungen 4 bis 6 zu sehen ist. Somit kann geschlussfolgert werden, dass die einzelnen Komponenten die Intensität lediglich vernachlässigbar schwächen, da die LED-Pflanzlampen über eine starke Leuchtkraft verfügen und somit der Bioreaktor in seiner Funktion nicht eingeschränkt wird. Dies konnte auch im laufenden Betrieb festgestellt werden, da die Algen eine hohe Wachstumsrate aufwiesen, wie Sibylle Fischer in ihrer Arbeit im Rahmen dieser Forschungsreihe nachwies. Trotzdem wäre es interessant eine Messung der LED-Pflanzlampe auf Stufe neun mit einem geeignetem Photospektrometer durchzuführen, da hier das genaue Spektrum bestimmt werden kann. Möglicherweise sind dann einzelne Spektralbereiche intensiver oder schwächer ausgeprägt.
Abbildung 7 zeigt, dass das Absorptionsspektrum von Chlorophyll A und B im roten Spektralbereich der LED-Pflanzlampen liegt. Die beiden Absorbtionsmaxima von Chlorophyll A und B im UV bis blauen Spektrum liegen nicht direkt im Maximum der LED-Pflanzlampe des gleichen spektralen Bereichs. Jedoch sind Überlappungen der Absorptionsmaxima zu erkennen. Auch sind Messungenauigkeiten des Spektrometers nicht auszuschließen. Dadurch und durch beobachtete und nachgewiesene Wachstum der Algen ist davon auszugehen, dass die LED-Pflanzlampen für diesen Bioreaktor geeignet sind.
¶ Zusammenfassung
Wie in der Einleitung dargelegt, sollte ein Versuchsaufbau zur Gewinnung von Wasserstoff mit Hilfe von Algen erstellt werden. Hierbei liegt der Fokus auf den mechanischen und optischen Aspekt, nicht auf der Erstellung der Nährlösung.
Die Konstruktion zum Algenanbau basiert auf einem Holzgerüst, einer Glasplatte, LED-Pflanzlampen, Plastikboxen sowie Schottflaschen. Sie wird mit Hilfe von Relais, einem Microcontroller und einer Programmierung in der Programmierumgebung „Arduino-DIE“ gesteuert. Die lichtgebenden LED-Pflanzlampen haben neun verschiedene Stärken, mit Stärke neun als höchste Stufe.
Der Kernaufbau kann eine reine, luftdichte Nährstoffversorgung der Algen sicherstellen. Die Lichtversorgung ist durch die Anordnung der Glasplatte und der Boxen nicht sonderlich beeinträchtigt. Allein die Begrenzung des Spektrometers hat eine volle Leistungsgebung und Auswertung der LED-Pflanzlampen verhindert.
Zusammenfassend kann man sagen, dass der Versuchsaufbau des Bioreaktor für den Forschungszweck zur Produktion von Wasserstoff durch Algen genutzt werden kann.
¶ Danksagung
An dieser Stelle möchte ich mich bei all denjenigen bedanken, die mich während der Anfertigung dieser Seminararbeit unterstützt und motiviert haben.
Insbesondere möchte ich mich bei Barbara Menz für die hilfreichen Anregungen und die konstruktive Kritik bei der Erstellung dieser Arbeit bedanken.
Auch gebührt mein Dank dem Mint-Labs Regensburg e.V., die mir die nötigen Materialien zur Verfügung gestellt haben.
Auch möchte ich Frau Ortner-Traxinger für das Ausleihen des Spektrometers danken.
Daneben gebührt auch Volkmar Gerhardt ein Danke für seinen wissenschaftlichen Diskurs.
¶ Anhänge
Box für Algen: https://www.hygi.de/emsa-clip-close-frischhaltedose-rechteckig-hochformat-fassungsvermoegen-1100-ml-pd-65707
Kabelverschraubung: https://www.amazon.de/Kabelverschraubung-Gorffy-Stück-Kabelverschraubungen-Kabeldurchführungen/dp/B0D7CH1KNV?source=ps-sl-shoppingads-lpcontext&ref_=fplfs&smid=A2LFHJ515YDVT&th=1
Peristaltikpumpe: https://www.amazon.de/dp/B0BLHYL1L7?ref=fed_asin_title
Luftpumpe, Schläuche, Saugnäpfe, Luftsteine und Rücklaufventile: https://www.amazon.de/gp/product/B0C5C8BG4S/ref=ox_sc_act_title_1?smid=A1QXLTHY5ONG05&psc=1
Schottflasche: https://www.laboratoriumdiscounter.nl/de/gewindeflasche-duran-pressure-plus.html
5V Relais-Modul: https://funduinoshop.com/bauelemente/taster-und-schalter/relais/4-kanal-relais-modul-5v
Die Glasplatte sowie das Holz für das Gerüst entstammen den Restbeständen der Mint-Labs Regensburg e.V.
Das verwendete Gefäß für den überlauf ist eine alte Vase aus Glas.
¶ Anhang 2
| Pumpe 1 | Pumpe 2 | Pumpe 3 | Durchschnitte pro 1min pumpen: | Standardabweichung in %: | Zeit um 5ml zu pumpen in Sekunden: | In Millisekunden: | |
| 176 | 154 | 141 | Pumpe 1 | 176 | 1,016394535 | 1,704545455 | 1704,545455 |
| 176 | 155 | 146 | Pumpe 2 | 155,6363636 | 1,325304 | 1,927570093 | 1927,570093 |
| 175 | 152 | 147 | Pumpe 3 | 148 | 2,112799892 | 2,027027027 | 2027,027027 |
| 174 | 154 | 148 | |||||
| 173 | 156 | 148 | |||||
| 176 | 157 | ||||||
| 176 | 154 | 148 | |||||
| 175 | 156 | 149 | |||||
| 178 | 158 | 150 | |||||
| 178 | 157 | 150 | |||||
| 179 | 159 | 153 |
¶ Anhang 3
#include <Wire.h>
#include <RTClib.h>
#include <LCDI2C_Multilingual_MCD.h>
RTC_DS3231 rtc; //Uhr
LCDI2C_Latin lcd(0x27, 16, 2); //Display
const int pump1Pin = 2;//Relais
const int pump2Pin = 3;
const int pump3Pin = 4;
const int tasterPin1 = 5;
const int tasterPin2 = 6;
const int relais4_6 = 7;
const int relais5_7 = 8;
int buttonState1 = 0;
int buttonState2 = 0;
void setup() {
lcd.init(); //Display initialisierung
lcd.backlight(); // Schalte die Hintergrundbeleuchtung ein
lcd.setCursor(0, 0); // Setze den Cursor auf die erste Zeile, erste Spalte
lcd.print("Uhrzeit:"); // Zeige "Zeit" auf dem Display an
Serial.begin(9600);
pinMode(pump1Pin, OUTPUT); //Pumpe3
pinMode(pump2Pin, OUTPUT); //Pumpe2
pinMode(pump3Pin, OUTPUT); //PUmpe1
pinMode(relais4_6, OUTPUT);
pinMode(relais5_7, OUTPUT);
pinMode(tasterPin1, INPUT_PULLUP);
pinMode(tasterPin2, INPUT_PULLUP);
if (!rtc.begin()) {
Serial.println("RTC nicht gefunden!");
while (1);
}
if (rtc.lostPower()) {
rtc.adjust(DateTime(2025, 4, 1, 14, 55, 0));
} //Jahr, Monat, Tag, Stunde, Minute, Sekunde
}
void loop() {
buttonState1 = digitalRead (tasterPin1);
buttonState2 = digitalRead (tasterPin2); // Auslesen vom Taster-Status
// Check ob der Taster gedrückt wird
Serial.print("Taster1: ");
Serial.print(buttonState1);
Serial.print(" | Taster2: ");
Serial.println(buttonState2);
if (buttonState1 == LOW && buttonState2 == LOW) {
// Beide gedrückt → alles aus
digitalWrite(relais4_6, LOW);
digitalWrite(relais5_7, LOW);
}
else if (buttonState1 == LOW) {
// Nur Taster1 gedrückt
digitalWrite(relais4_6, HIGH);
digitalWrite(relais5_7, LOW);
}
else if (buttonState2 == LOW) {
// Nur Taster2 gedrückt
digitalWrite(relais5_7, HIGH);
digitalWrite(relais4_6, LOW);
}
else {
// Keiner gedrückt
digitalWrite(relais4_6, LOW);
digitalWrite(relais5_7, LOW);
}
DateTime now = rtc.now();
// Ausgabe der aktuellen Uhrzeit auf dem seriellen Monitor
if (now.second() == 0){
Serial.print("Zeit: ");
Serial.print(now.hour());
Serial.print(":");
Serial.print(now.minute());
Serial.print(":");
Serial.print(now.second());
Serial.println(); // Neue Zeile
}
if (now.minute() == 0 && now.second() == 0) {
digitalWrite(pump1Pin, HIGH);
digitalWrite(pump2Pin, HIGH);
digitalWrite(pump3Pin, HIGH);
lcd.setCursor(0,0);
lcd.print("Es wird gepumpt!");
lcd.setCursor(0,1);
lcd.print(" ");
delay(1704);
digitalWrite(pump3Pin, LOW);
delay(223);
digitalWrite(pump2Pin, LOW);
delay(100);
digitalWrite(pump1Pin, LOW);
Serial.println("Es wurde gepumpt!");
}
//Gibt Uhrzeit am I2C Display aus
lcd.setCursor(0,0);
lcd.print("Uhrzeit:");
lcd.print(" ");
lcd.setCursor(0,1);
lcd.print(now.hour());
lcd.print(":");
lcd.print(now.minute());
lcd.print(":");
lcd.print(now.second());
lcd.print(" "); // Ansonsten bleibt eine 9 immer hängen
delay(60);
}
¶ Anhang 4
Bei der verwendeten Software handelt es sich um SpectraLab von LEYBOLD, das als Systemanforderung Windows XP/Vista/7/8/10/11 benötigt.
Bei dem verwendeten Spektrometer handelt es sich um das Kompakt-Spektrometer 467251 von LEYBOLD.